导览
近日,癌症免疫治疗学会(sitc)第38届年会于11月1日-11月5日在美国圣迭戈召开,斯丹赛生物技术有限公司(以下简称斯丹赛)受邀参加本次年会。斯丹赛高级副总裁田乐博士代表公司出席,并在会上以壁报形式展示了斯丹赛基于自主研发的coupledcar平台技术开发的首发候选产品gcc19cart,该产品被开发用于治疗复发/难治性转移性结直肠癌(r/r mcrc)患者。
癌症免疫治疗学会成立于1984年,是世界领先的致力于通过推进癌症免疫治疗科学与应用来改善癌症患者预后的非营利组织。sitc的愿景是通过促进科学交流与合作教育计划,旨在让癌症患者在某一天被“治愈”成为现实。这与斯丹赛的愿景不谋而合,斯丹赛专注于开发用于治疗实体瘤的细胞免疫疗法,致力于利用创新的细胞治疗技术治愈晚期肿瘤患者。
斯丹赛展示的壁报信息
标题:a phase 1 dose escalation study of gcc19cart – a novel coupledcar® therapy for subjects with metastatic colorectal cancer(gcc19cart的i期剂量递增研究——一种用于转移性结直肠癌受试者的新型coupledcar®疗法)
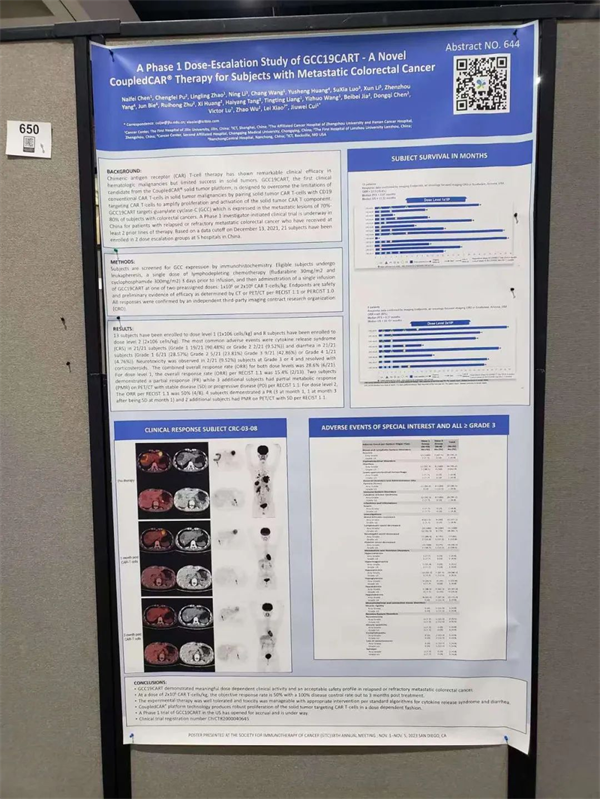
初步临床疗效已优于标准疗法
斯丹赛gcc19cart的i期剂量递增研究,是在中国进行的由研究者发起的一项多中心的剂量爬坡临床试验,21名受试者分别被随机分配到2个剂量组中,这些患者在入组前均接受了二线及以上的治疗。其中13名受试者被纳入低剂量组(1x10^6 cart/kg),8名受试者被纳入中剂量组(2x10^6 cart/kg)。根据实体肿瘤疗效评价标准(recist1.1),低剂量组客观缓解率为15.4%(2/13),中剂量组客观缓解率为50%(4/8),中剂量组的中位随访时间(mos)已经超过24个月,明显优于fda批准的标准疗法的三线药物(mos仅为6-8个月)。该项研究的初步结果显示,gcc19cart在复发/难治性转移性结直肠癌患者中显示出与剂量相关的良好的临床初步疗效以及可控的安全性。
gcc19cart已获得美国食品和药物管理局(fda)的临床试验批件,已开始在美国的临床试验,该临床试验与美国几家顶级医疗中心合作进行,目前试验进展顺利。
全球领先的coupledcar实体瘤car-t平台技术
car-t细胞疗法在血液瘤恶性肿瘤中已展现出显著的临床疗效,但在实体肿瘤中的治疗效果仍然有限。斯丹赛经过多年潜心研制,打造了专攻实体瘤car-t的coupledcar平台技术,并结合新筛选出的肿瘤特异表达且安全的靶点,来治疗多种实体瘤。coupledcar平台技术的核心一是使用双重car方法来刺激免疫系统,以促进car-t细胞扩增;二是增强了与t细胞迁移相关的基因表达,改善了car-t细胞向肿瘤迁移和浸润受到抑制的困境;三是增强了car-t细胞在肿瘤微环境中的杀伤能力,进入实体瘤后,coupledcar可刺激机体产生、募集更多的免疫细胞,引发更有效和持久的反应。coupledcar平台技术解决了实体瘤car-t细胞难以进入到实体肿瘤内部、难以在体内扩增、以及难以对肿瘤细胞造成杀伤的难题。斯丹赛在car-t技术领域已有三百余项全球专利及专利申请。
此外,coupledcar是一种平台技术,可扩展到其他多个实体瘤靶点和适应症,目前已在前列腺癌临床试验中展现临床疗效。以pap为靶点的前列腺癌产品papcart正在推进国内临床试验,已回输的4例受试者中有3例达到了psa应答(注:psa应答指前列腺癌特异标志物psa水平和基线相比,下降50%以上)。前列腺癌产品的疗效进一步证明了coupledcar作为平台技术的可扩展性很好,未来可以治疗更多其他适应症,惠及更多病人。
关于斯丹赛
斯丹赛生物技术有限公司是一家专注于开发用于治疗实体瘤的细胞免疫疗法的生物制药公司。斯丹赛独特的coupledcar平台技术旨在克服治疗实体瘤的关键挑战,基于该平台技术开发的car-t产品已经在治疗晚期实体瘤(如结直肠癌)中取得了可喜的临床结果。公司针对晚期结直肠癌的car-t细胞治疗产品gcc19cart于2021年8月获得了美国食品和药物管理局(fda)的临床试验批件,并于2022年4月获得fda授予的快速通道资格,目前已开始美国的临床入组。斯丹赛同时也在布局针对其它实体瘤(包括前列腺癌、胰腺癌等)的丰富的car-t候选药物管线。欲了解更多信息,请访问www.ictbio.com。
免责声明:市场有风险,选择需谨慎!此文仅供参考,不作买卖依据。
关键词: